São agentes oxidantes de uso frequente: oxigênio gasoso (O2), oxidante natural, o ozônio (O3), em reações de ozonólise, o permanganato de potássio (KMnO4) e o dicromato de potássio (K2 Cr2 O7).
OXIDAÇÃO DE ÁLCOOIS
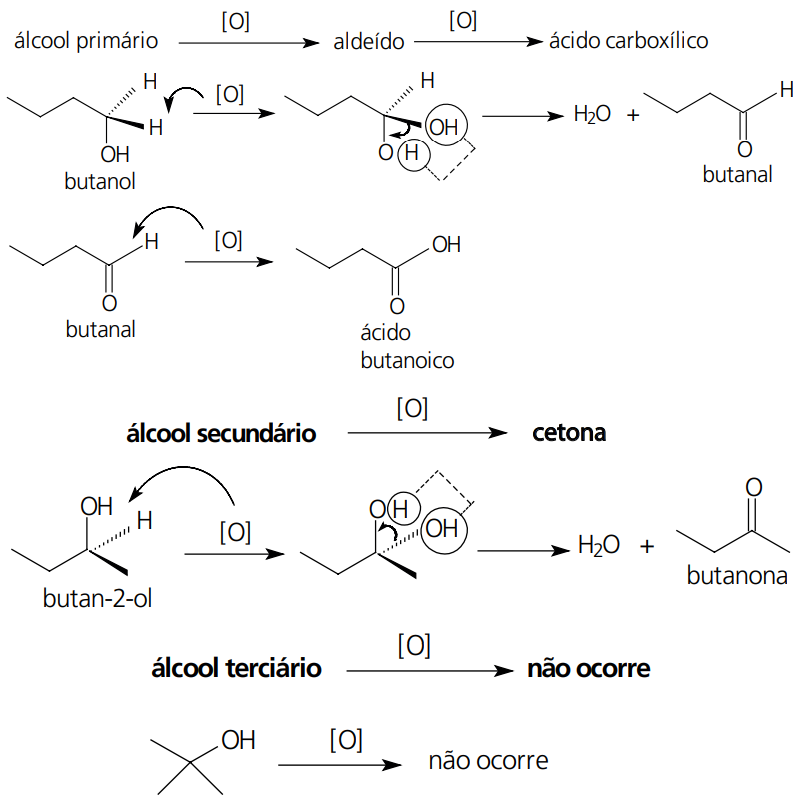
Observação: os álcoois primários são oxidados a aldeídos, sem se transformar em ácidos carboxílicos, por composto de Cromo IV, na ausência de água e na presença de solventes como a piridina.
OXIDAÇÃO DE ALCENOS E CICLENOS
OXIDAÇÃO BRANDA
Quando tratamos um alceno com uma solução aquosa diluída de permanganato de potássio em meio básico ou neutro ocorre uma oxidação branda. Nela verificamos a conservação do número original de átomos de carbono e o surgimento de duas hidroxilas nos carbonos da dupla formando um diol vicinal. Reação com permanganato em meio básico ou neutro: O permanganato em meio básico ou neutro é brando, pois não rompe a cadeia na posição da dupla ligação, porém introduz radicais hidroxilas na cadeia.
oxidação branda. Nela verificamos a conservação do número original de átomos de carbono e o surgimento de duas hidroxilas nos carbonos da dupla formando um diol vicinal. Reação com permanganato em meio básico ou neutro: O permanganato em meio básico ou neutro é brando, pois não rompe a cadeia na posição da dupla ligação, porém introduz radicais hidroxilas na cadeia.
Observação: essa reação é conhecida como Teste de Bayer, que serve para a identificação de ligação dupla entre carbonos nos compostos.
OXIDAÇÃO ENÉRGICA
Quando tratamos um alceno com uma mistura de permanganato de potássio com ácido sulfúrico (mistura sulfomangânica) ou dicromato de potássio com ácido sulfúrico (mistura sulfocrômica) ocorre uma oxidação enérgica. Nela verificamos a ruptura total da molécula na região da ligação dupla. Cada carbono da dupla recebe um átomo de oxigênio formado um grupamento carbonila, formando aldeídos e/ou cetonas. Os aldeídos formados são posteriormente oxidados a ácidos carboxílicos. O carbono da extremidade presente nas cadeias carbônicas dos alcenos (que apresentam ligação dupla) são oxidados a dióxido de carbono e água.
REAÇÃO COM PERMANGANATO OU DICROMATO EM MEIO SULFÚRICO
Essas oxidações são consideradas enérgicas. Além de romper a molécula do alceno na região da dupla ligação, verificamos a oxidação de aldeídos formados a ácidos carboxílicos.
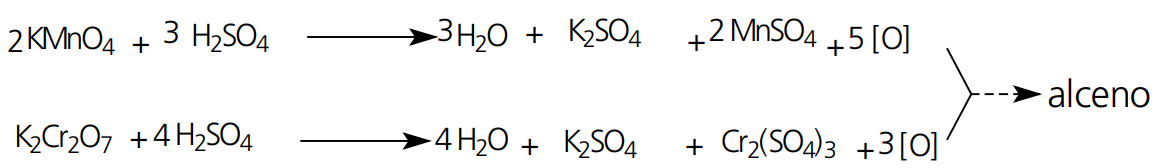
Exemplos:
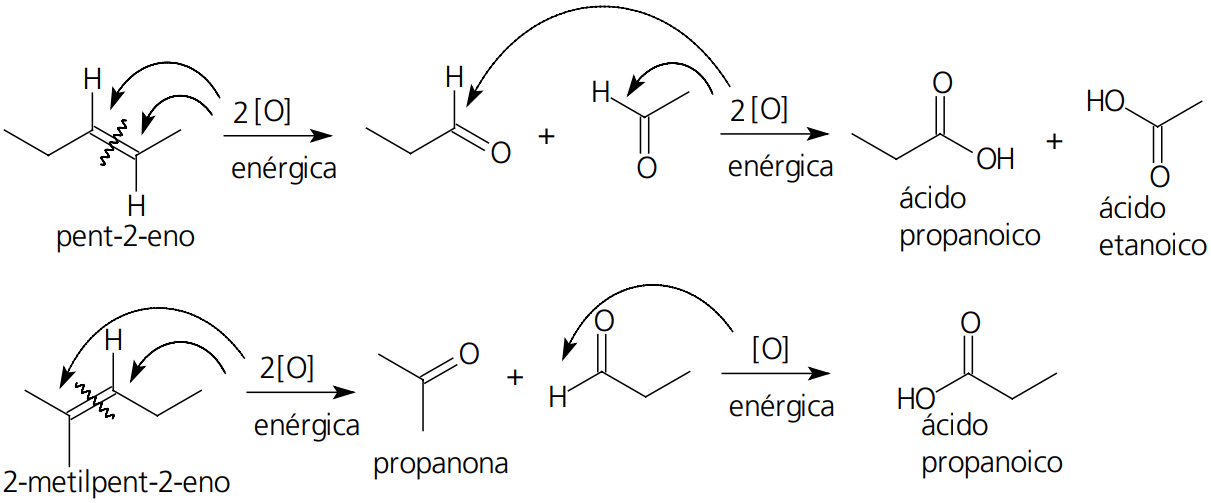
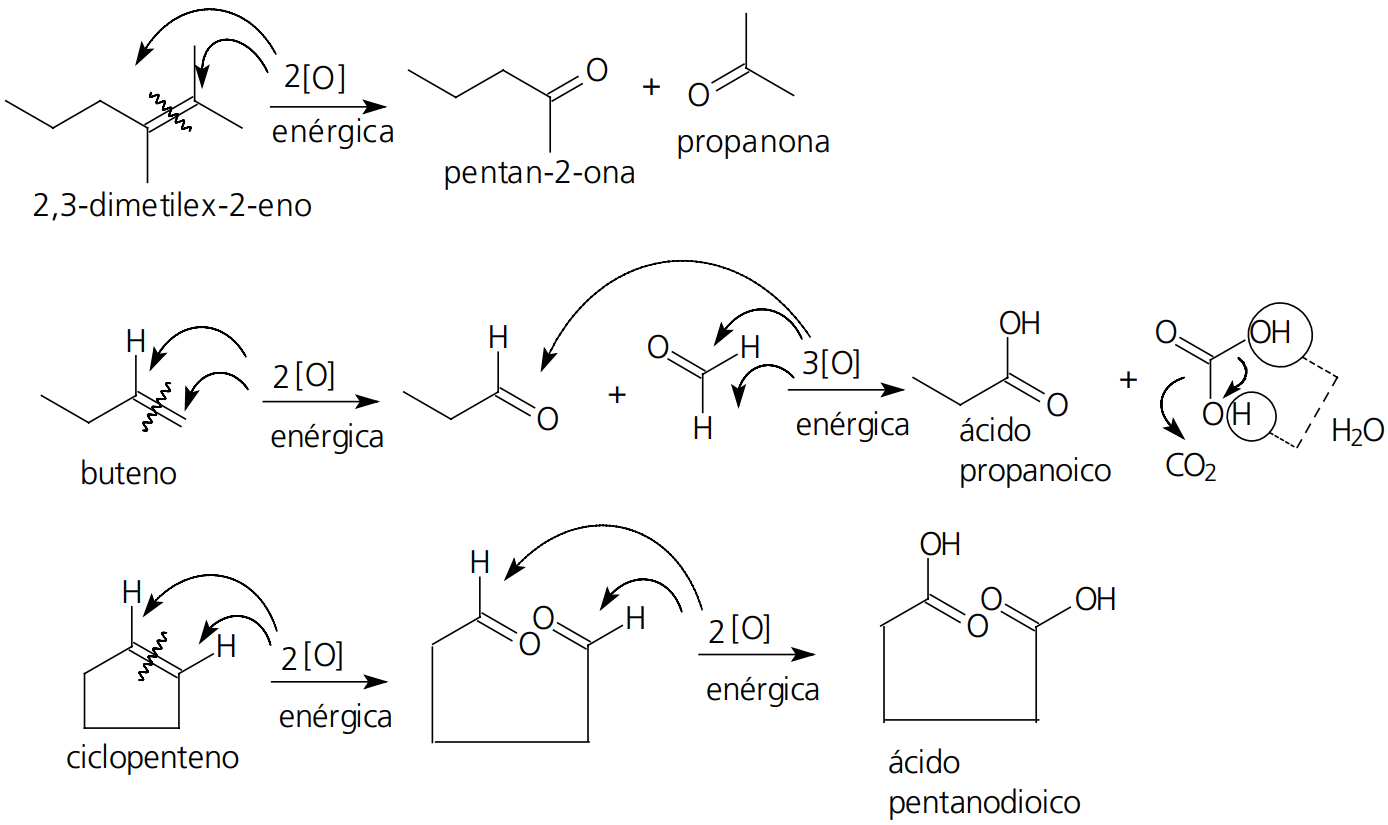
OXIDAÇÃO ENÉRGICA DE ALCINOS, ALCADIENOS E CICLANOS
ALCINOS
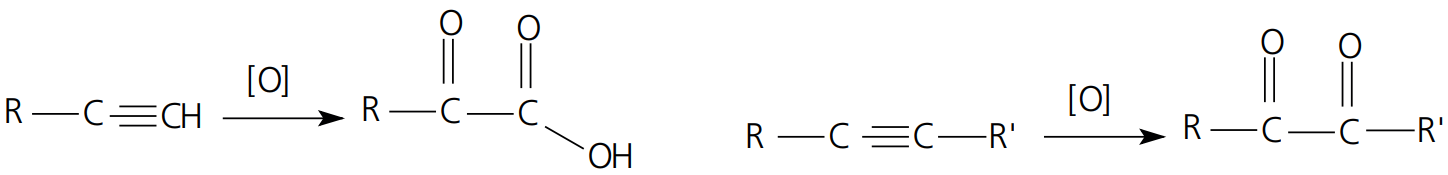
ALCADIENOS
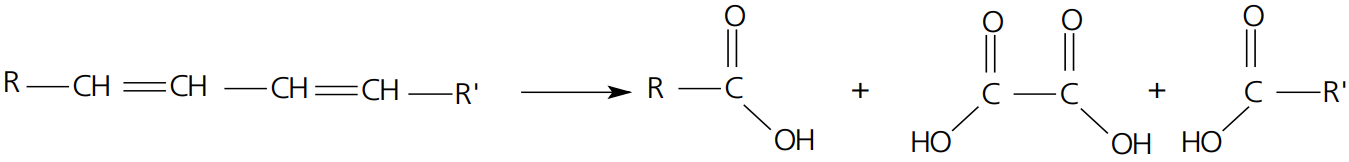
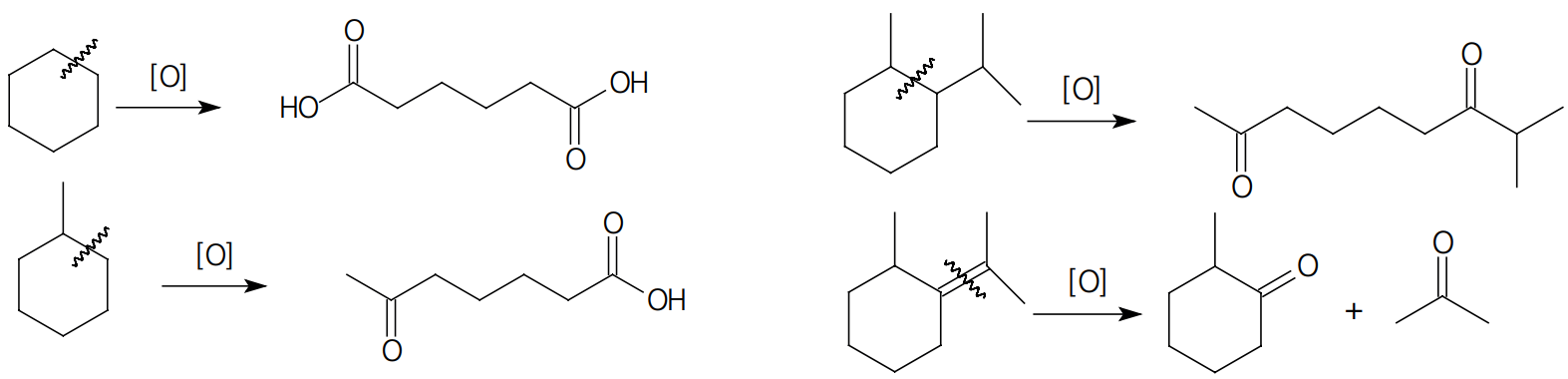
CICLANOS
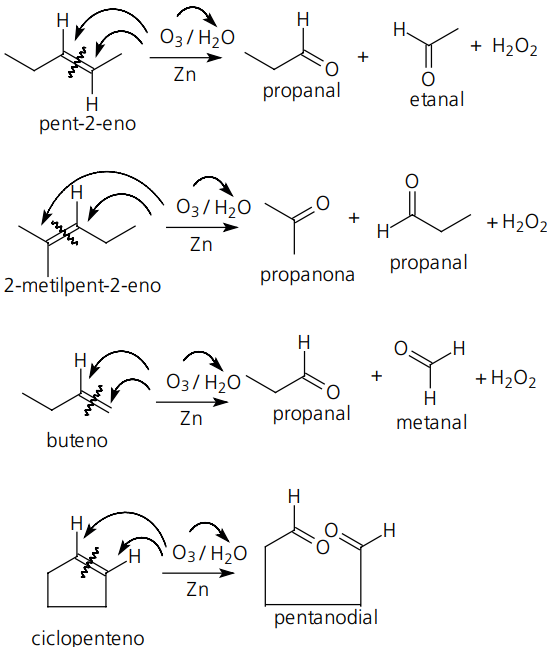
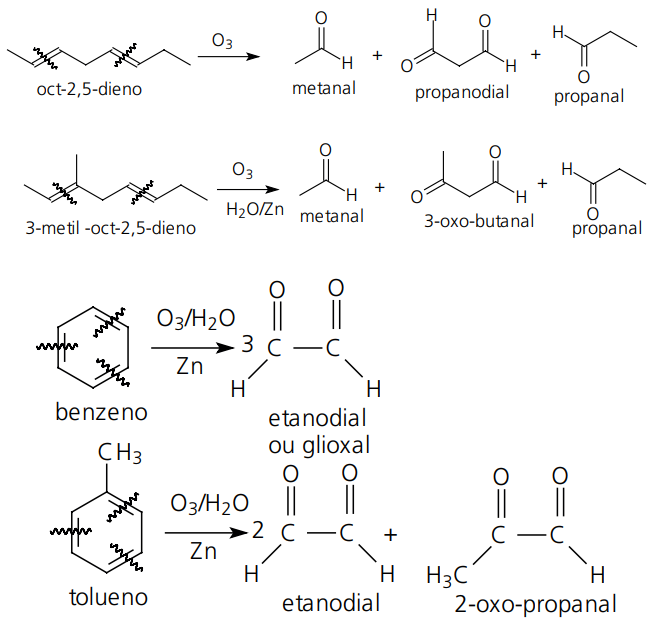
OZONÓLISE
É um tipo de oxidação mais forte do que a branda, porém mais fraca do que a enérgica. O composto (alceno ou cicloalceno, por exemplo) é tratado com ozônio, água e zinco em pó. A reação se processa com a ruptura da molécula na regiāo da ligação dupla. Cada carbono da dupla recebe um átomo de oxigênio formado um grupamento carbonila, formando aldeídos e/ou cetonas. Os aldeídos formados não são posteriormente oxidados a ácidos carboxílicos devido à presença do zinco que atua como inibidor.