PRESSÃO MÁXIMA DE VAPOR DE UM LÍQUIDO PURO NUMA DADA TEMPERATURA (PV)
Considere um líquido puro, a temperatura constante num sistema fechado:
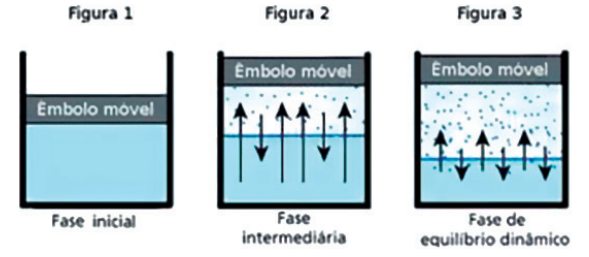
A pressão máxima de vapor (ou pressão de vapor) de um líquido é a pressão exercida pelo seu vapor quando este se encontra em equilíbrio com sua fase líquida.
CURVA DE VAPORIZAÇÃO DE UM LÍQUIDO
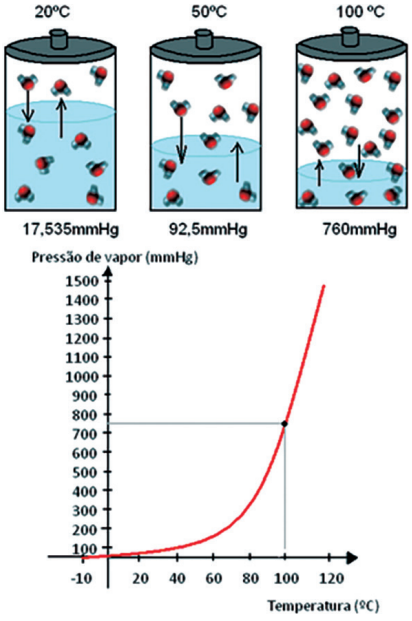
Observação 1: Quando aquecemos um líquido puro, a sua pressão de vapor pode aumentar até o valor da pressão atmosférica local (1 atm ou 760 mmHg, por exemplo).
Observação 2: Podemos então afirmar que o líquido atingiu a sua temperatura ou ponto de ebulição (Te).
Observação 3: Na altitude, onde é menor a pressão atmosférica, a temperatura de ebulição dos líquidos é menor do que ao nível do mar, local de pressão atmosférica máxima.
Observação 4: O que chamamos de fervura, saída de bolhas do líquido quando se encontra em ebulição, se deve ao fato de que em determinadas regiões do recipiente em que o líquido está sendo aquecido, a densidade do mesmo ficou menor do que na região em que ele está frio, sendo assim, ocorre um deslocamento do líquido quente, e também do vapor para a região fria, condução de calor por convecção, provocando o borbulhamento.
PRESSÃO DE VAPOR × VOLATILIDADE DOS LÍQUIDOS
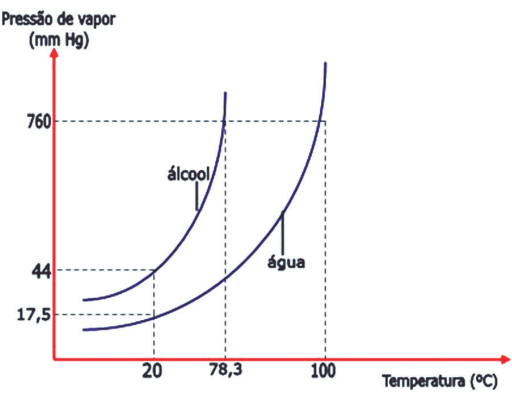
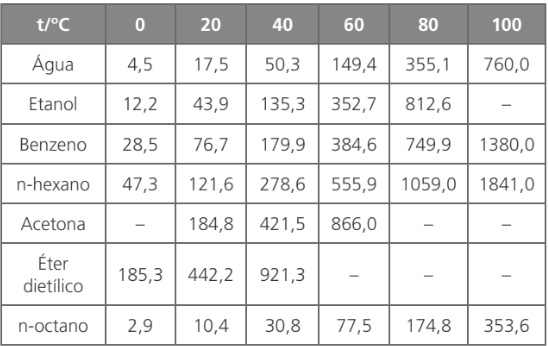
(Pv)álcool > (Pv)água → (Te)álcool < (Te)água
– O álcool é o líquido mais volátil.
– A água é o líquido mais fixo.
Observação: o tratamento físico químico da pressão de vapor e/ou da temperatura de ebulição dos líquidos serve como fundamentos para explicar as questões relacionadas às forças intermoleculares existentes nas substâncias analisadas como fator de influência desse comportamento.
RELAÇÃO ENTRE PRESSÃO DE VAPOR E TEMPERATURA DE EBULIÇÃO (EQUAÇÃO DE CLAUSIUS – CLAPEYRON)

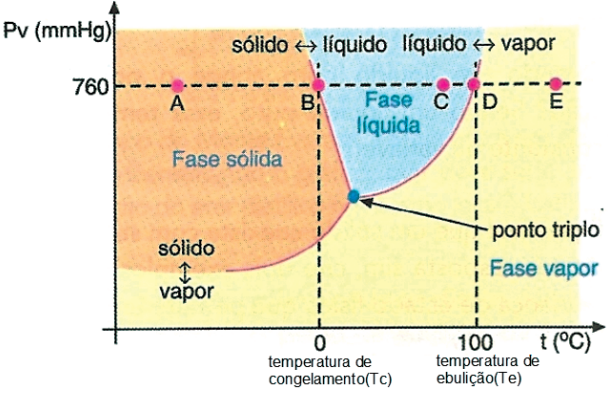
DIAGRAMA DE FASES DA ÁGUA