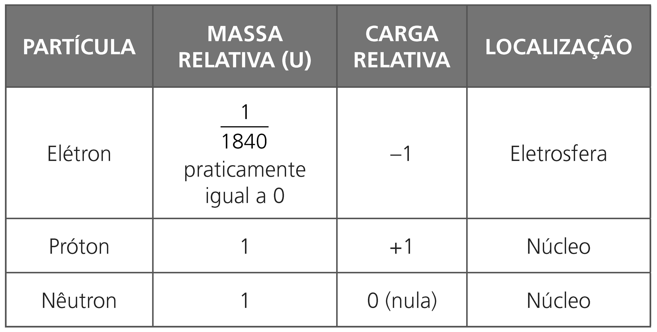
Foram atribuídos os seguintes valores para as cargas e massas relativas dos prótons, nêutrons e elétrons:
NOTA COMPLEMENTAR
- É a diferente quantidade das partículas formadoras dos átomos que ocasiona as diferenças entre eles.
- O número de prótons de um átomo é a característica mais importante. Diferenças de números de prótons dão diferenças químicas entre átomos.
- O número de nêutrons constitui característica de importância relativa. Diferença somente no número de nêutrons, por exemplo, não conduz a diferenças químicas entre os átomos.
- A carga elétrica de um próton ou de um elétron é 1,6·10-15 coulombs.
Os átomos diferem uns dos outros pelos números de prótons, elétrons e nêutrons que entram na sua formação. Na realidade, é o número de prótons do átomo que o caracteriza quimicamente, esse número é chamado de número atômico e é representado pela letra Z.
Número atômico (Z) é o número de prótons de um átomo.
O número de nêutrons de um átomo não interfere nas suas características químicas. Desse modo, átomos com diferentes números de nêutrons, mas com o mesmo número de prótons, são átomos do mesmo elemento químico.
A massa de um átomo é dada pelo seu número de prótons e nêutrons, pois a massa dos elétrons é desprezível em relação a dos prótons e nêutrons. O número de prótons, somado ao número de nêutrons de um átomo, é chamado número de massa e é representado pelo símbolo A.
Número de massa (A) de um átomo é o seu número de prótons somado ao seu número de nêutrons.
A = Z + N ou A = p + n
A notação geral de um átomo é:
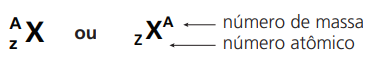
Exemplos:

Observação:
- Como o número atômico (Z) é o número de prótons (p) que o átomo possui, derivamos daí o atual conceito de elemento químico:
Elemento químico é um conjunto de átomos com o mesmo número atômico ou prótons.
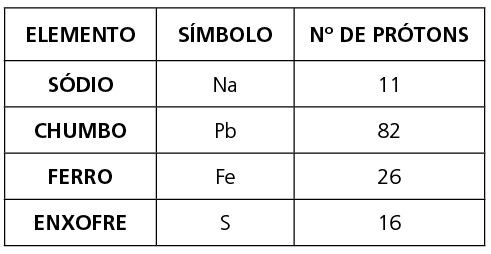
A cada elemento químico atribui-se um nome. A cada nome corresponde um símbolo e, consequentemente, a cada símbolo corresponde um número atômico.
- O núcleo é muito menor que a eletrosfera (10 mil vezes menor) e é mantido coeso por uma força nuclear que existe entre suas partículas.

Na eletrosfera, temos as partículas elétricas negativas: elétrons (e).
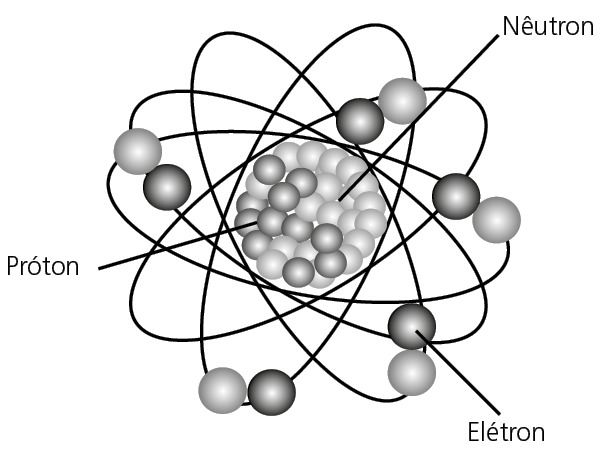
- Dimensões da eletrosfera: o diâmetro da eletrosfera também varia conforme o número de elétrons que o átomo possui e o estado de energia desses elétrons (fundamental ou ativado); porém, em média, o diâmetro da eletrosfera de um átomo fica em torno de 10-10 m (1 Å).
Comparando os diâmetros do núcleo e da eletrosfera do átomo, concluímos que a eletrosfera é algo entre dez mil e cem mil vezes maior que o núcleo.





