PERCENTUAL DE CARÁTER IÔNICO DE UMA LIGAÇÃO
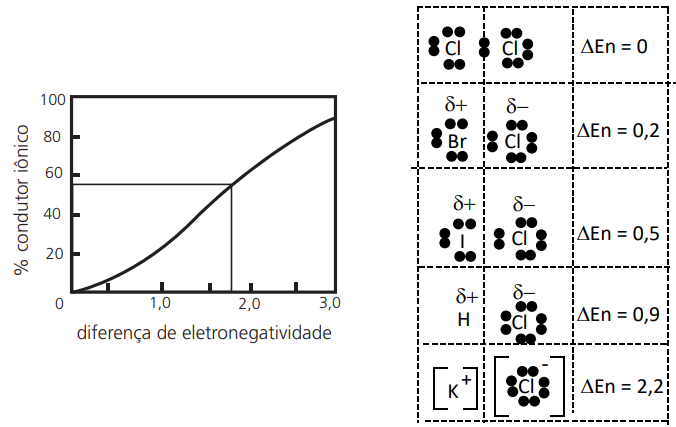
Mesmo apresentando características diferentes, a ligação iônica e a ligação covalente se confundem quanto ao posicionamento da nuvem eletrônica que envolve a estrutura da substância obtida. Uma forma de diferenciar essas ligações é através dos valores da variação de eletronegatividade (∆ En).
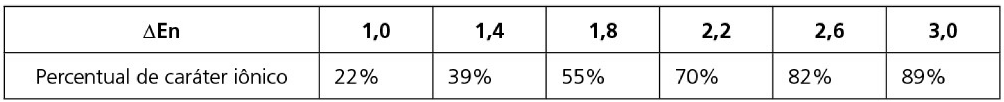
Uma avaliação mais lúcida é a avaliação pelo percentual de caráter iônico de uma ligação.
POLARIDADE DAS MOLÉCULAS
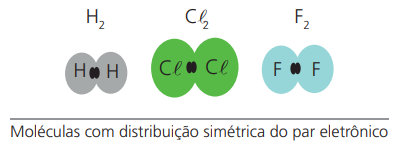
LIGAÇÃO COVALENTE APOLAR
Ocorre quando os átomos participantes apresentam o mesmo valor de eletronegatividade. Logo, a variação da eletronegatividade entre os átomos da ligação (∆ En) é igual a zero (∆En = 0).
LIGAÇÃO COVALENTE POLAR
Ocorre quando os átomos participantes apresentam diferentes valores de eletronegatividade (∆En ≠ 0). Essa molécula pode também ser denominada de DIPOLO.
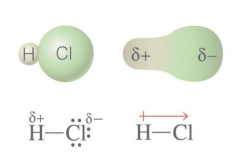
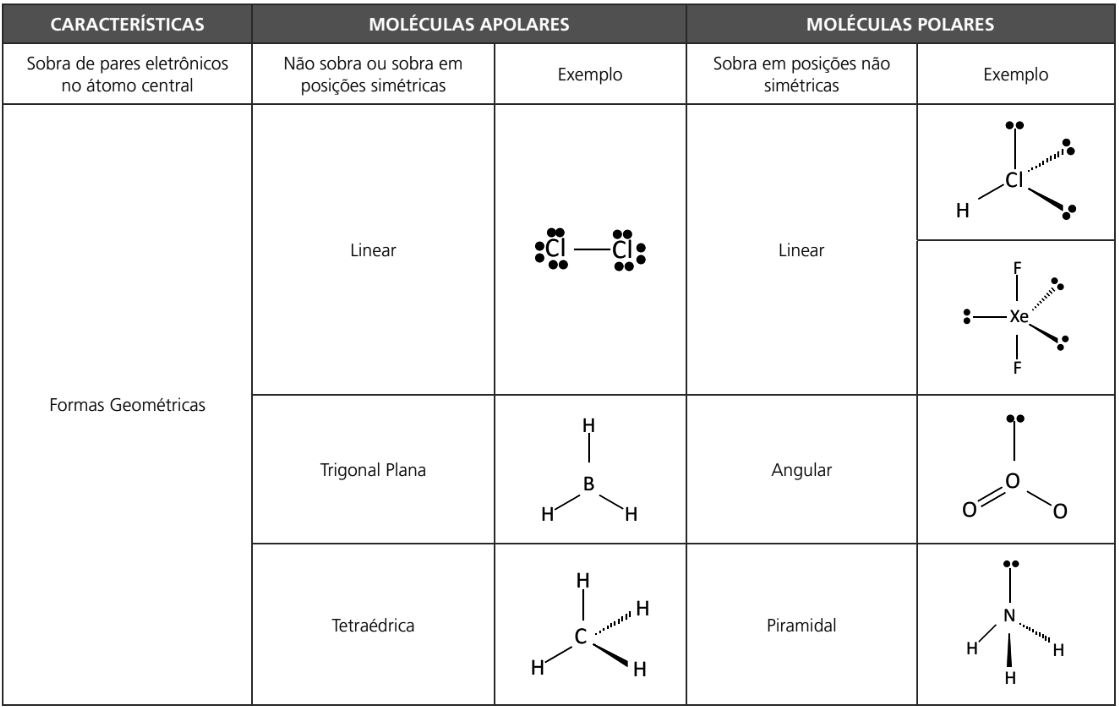
GEOMETRIA E POLARIDADE DAS MOLÉCULAS
As estruturas moleculares de geometria trigonal plana, tetraédrica, octaédrica e bipirâmide trigonal podem sofrer alterações de sua geometria (deformação) quando o número de ligantes da estrutura original se reduz e, consequentemente, verificamos a sobra de pares eletrônicos não ligantes no átomo central; esse fato irá influenciar na polaridade da molécula analisada.
TEORIA DA REPULSÃO DOS ELÉTRONS DA CAMADA DE VALÊNCIA (VSEPR)
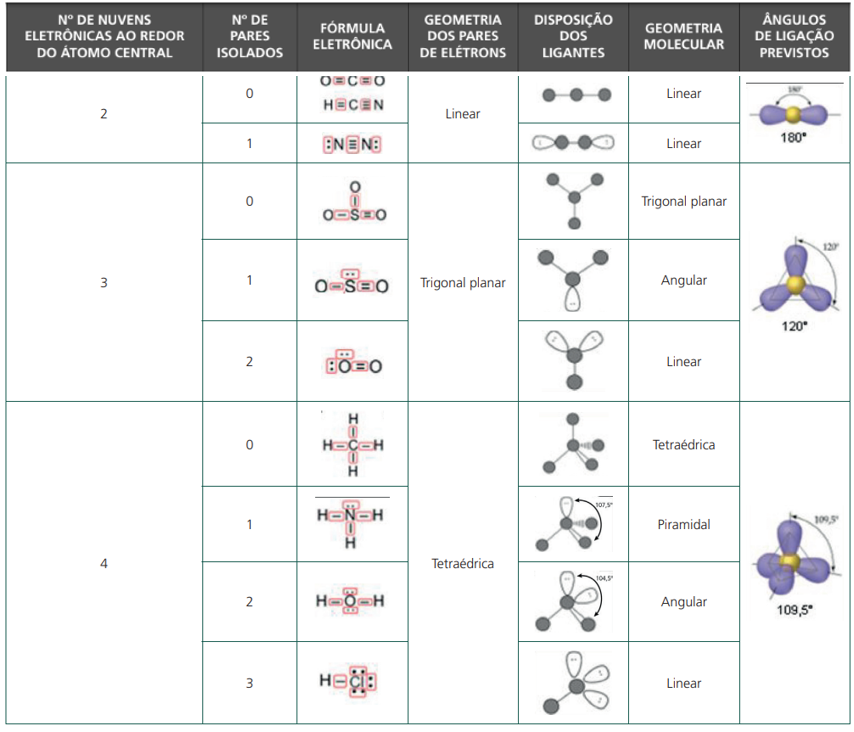
POLARIDADE DAS MOLÉCULAS